Theo VnExpress – Cục Quản lý Dược, Bộ Y tế, cấp phép khẩn cấp 3 loại thuốc chứa hoạt chất molnupiravir điều trị Covid-19 do doanh nghiệp Việt Nam sản xuất.
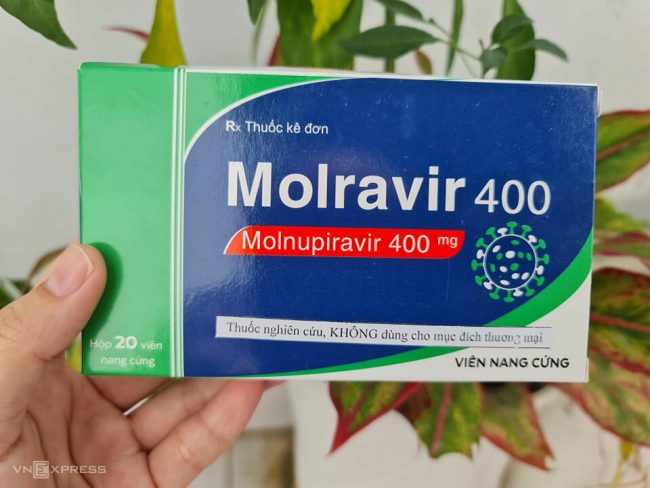
Đại diện Cục Quản lý Dược chiều 17/2 xác nhận thông tin trên và cho biết đã ban hành danh mục thuốc đi kèm. Theo đó, ba loại thuốc được cấp phép gồm Molravir 400 của Công ty Cổ phần Dược phẩm Boston Việt Nam, Movinavir hàm lượng 200 mg của Công ty Cổ phần Hóa – dược phẩm Mekorpha và Molnupiravir Stella 400 của Công ty TNHH Stellapharm.
Molnupiravir là hoạt chất có tác dụng kháng virus, được xem là “vũ khí” quan trọng trong điều trị F0 tại nhà. Thuốc có tác dụng giảm tải lượng virus khi sử dụng ở giai đoạn đầu mắc bệnh, từ đó giảm nguy cơ trở nặng và tử vong. Thuốc dạng viên, dùng theo đường uống, thuận tiện cho F0 tại nhà.
Như vậy, đây là thuốc kháng virus đầu tiên điều trị Covid-19 được cấp phép tại Việt Nam. Quyết định cấp phép khẩn cấp thuốc molnupiravir của Cục Quản lý Dược căn cứ đề xuất hôm 5/1 của Hội đồng Tư vấn cấp giấy phép lưu hành thuốc và nguyên liệu làm thuốc. Ba điều kiện đi kèm với đề xuất cấp phép khẩn cấp là doanh nghiệp phải kiểm tra chất lượng nguyên liệu đạt yêu cầu trước khi sản xuất; tiếp tục theo dõi, kiểm tra chất lượng thuốc hàng tháng sau khi được cấp giấy đăng ký lưu hành; tiếp tục nghiên cứu độ ổn định của thuốc và nộp dữ liệu nghiên cứu, hồ sơ cập nhật hạn dùng để thẩm định theo yêu cầu của Bộ hồ sơ kỹ thuật chung ASEAN.
Trả lời VnExpress, phó giáo sư, tiến sĩ Lê Văn Truyền, Chủ tịch Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc, cho rằng quyết định cấp phép thuốc molnupiravir sản xuất nội địa “rất ý nghĩa”. Theo đó, Việt Nam có thể tự túc thuốc kháng virus sản xuất trong nước, tiếp tục phòng chống Covid-19. Tổ chức bằng sáng chế thuốc (MPP) đã nhượng quyền sản xuất molnupiravir cho Việt Nam, tức là sẽ không gặp vấn đề về bản quyền và sản xuất thuốc này trong nước.
“Bộ Y tế sẽ xem xét cấp phép cho những doanh nghiệp sản xuất thuốc molnupiravir khác nếu bộ hồ sơ kỹ thuật đạt yêu cầu để sản xuất, nhằm tránh độc quyền cung cấp thuốc ra thị trường”, ông Truyền nói.
Hồi đầu tháng 1, có 10 doanh nghiệp nộp hồ sơ xin cấp phép thuốc molnupiravir. Hiện Bộ Y tế cấp phép cho 3 công ty, 7 đơn vị còn lại cần bổ sung hồ sơ để xem xét tiếp.
Ông Truyền cũng cho rằng thuốc được sản xuất trong nước sẽ giúp xác lập thị trường thuốc molnupiravir. Thời gian qua, thuốc chưa được cấp phép và do Bộ Y tế cấp phát cho F0, nên được rao bán tràn lan và hình thành thị trường kinh doanh bất hợp pháp với giá rất cao. Khi được cấp phép, thị trường thuốc molnupiravir sẽ được Bộ Y tế quản lý, kiểm soát giá.
Đến nay Bộ Y tế đã cấp hơn 300.000 liều thuốc molnupiravir cho Chương trình thí điểm điều trị có kiểm soát các trường hợp mắc Covid-19 thể nhẹ. Chương trình này được triển khai tại TP HCM từ giữa tháng 8 và đã mở rộng ra 51 địa phương có dịch. Kết quả thử nghiệm do Bộ Y tế công bố hồi tháng 11/2021, cho thấy gần 100% bệnh nhân dùng thuốc có tải lượng virus thấp, tỷ lệ chuyển nặng rất thấp, không có ca tử vong.
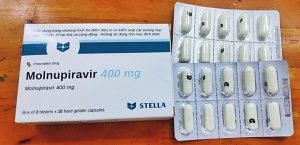
Molnupiravir cùng với favipiravir, remdesivir là 3 loại thuốc kháng virus đã được Bộ Y tế đưa vào phác đồ điều trị Covid-19 ở Việt Nam. Remdesivir là thuốc tiêm truyền tĩnh mạch, dùng cho bệnh nhân nặng, chỉ sử dụng trong bệnh viện.
Theo quy định, thuốc và vaccine phải trải qua quá trình thử nghiệm lâm sàng với 3 giai đoạn, theo dõi nghiêm ngặt, trước khi được cấp phép. Trong bối cảnh Covid-19 bùng phát rộng trên toàn thế giới, thuốc và vaccine được cấp phép khẩn cấp với các điều kiện ngặt nghèo, để đáp ứng yêu cầu cấp bách phòng chống dịch bệnh. Sau khi được cấp phép khẩn cấp, thuốc và vaccine vẫn tiếp tục được nghiên cứu đến khi hoàn tất, đủ điều kiện xin cấp phép toàn diện.
Hồi cuối tháng 12/2021, Công ty Cổ phần Hóa – dược phẩm Mekophar nhận một tấn nguyên liệu từ Ấn Độ để bào chế hơn 4,7 triệu viên molnupiravir. Hôm 20/1, Công ty Stellapharm được Tổ chức Bằng sáng chế Thuốc nhượng quyền sản xuất molnupiravir, cung cấp 105 quốc gia thu nhập thấp và trung bình.